آب مقطر
نگاه کلی:
آب طبیعی به علت خاصیت حل کنندگی خوبی که دارد معمولا دارای حجم بالایی از نمکهای محلول در آب میشود. CO2 هوا به خاطر انحلال در آب و تولید اسید کربنیک ضعیف ، خاصیت خورندگی آب را بهبود میبخشد. بنابراین آب هنگام عبور از محیطهای گوناگون مخصوصا محیطهای آهکی مقداری از کربناتها را در خود حل میکند که این کربناتها همراه یونهایی مثل کلسیم ، منیزیم و … باعث ایجاد سختی موقت میشود که با جوشاندن از بین میرود. البته یونهای منیزیم و کلسیم و سایر یونهای فلزی با سولفات و نیترات و کلرو ایجاد سختی دائم میکنند. سختی آب باعث رسوب کردن صابون در آب میشود (خاصیت کف کنندگی صابون را از بین میبرد)
اثرات زیانبخش ناخا لصیهای آب در صنعت :
آب در شیمی یکی از مهمترین حلالها میباشد و معمولا از آن به عنوان حلال عمومی نام میبرند و بنابراین کاربرد اساسی در صنعت دارد که برخی از کاربردهای مهم به این شرح میباشد:
- به عنوان حلال
- به عنوان ماده اولیه برای شرکت در واکنشهای شیمیایی تهیه محصول
- به عنوان ماده واسطه برای خارج کردن مواد ناخواسته
- به عنوان بستر یا محیط واکنش
وجود ناخالصیها در آب باعث ایجاد رسوب در دستگاههای حرارتی و دیگ بخار میشود که این عمل باعث کاهش عمر مفید دستگاه میگردد. بخاری که از آبهای ناخالص تولید میشود دارای کیفیت بسیار پایینی میباشد به عنوان مثال سیلیس همراه بخار خارج شده و در اثر سرد شدن روی پرههای توربین رسوب میکند. خوردگی بویلرها و تأسیسات حرارتی و لولهها ، اتلاف مواد شیمیایی و باقی گذاشتن لکه روی محصولات غذایی و نساجی از عوارض دیگر آبهای ناخالص میباشد.
بهترین آب برای استفاده در صنعت آب بدون یون است اما هزینه تولید آب بدون یون بسیار بالاست. بنابراین در اکثر آزمایشگاهها و واحدهای صنعتی از آب مقطر استفاده میکنند همچنین در مناطق کویری و خشک که منابع آب آشامیدنی محدود میباشد. از روش تقطیر آب دریا برای تولید آب آشامیدنی استفاده میشود.
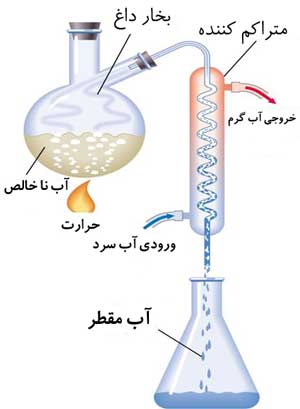
روش تقطیر آب
تقطیر یک محصول و خالص سازی آن به فراریت اجزای آن محلول یعنی اختلاف نقاط جوش آنها بستگی دارد. آب طبیعی از دو جزء حلال (آب) و مواد حل شده (انواع نمکها) تشکیل شده است. آب جزء فرار میباشد. در اثر حرارت آب بخار میشود و نمکهای موجود در آن در ظرف تقطیر به صورت رسوب باقی میماند. اگر بخار آب حاصل را سرد کنیم بخار به مایع تبدیل شده و آب مقطر به دست میآید. با تکرار تقطیر میتوان آب مقطر با خواص بهتری را بدست آورد.
از آب مقطر به دست آمده در آزمایشگاههای شیمی بطور گسترده استفاده میشود همچنین آب مقطر استریل شده در تزریقات کاربرد فراوانی دارد. آب مقطر مانند آب آشامیدنی گوارا نمیباشد. زیرا مقداری از اکسیژن محلول و همچنین برخی از یونهایی که باعث ایجاد طعم خوب آب میشود را از دست داده است. در تاسیسات آب شیرین کن بعد از اینکه آب شور را تقطیر کرده و آب مقطر تولید میکنند طی فرآیندهایی که روی آب انجام میدهند طعم آن را بهبود بخشیده و برای نوشیدن مناسب میسازند.
برخی خواص آب مقطر :
PH آب مقطر خنثی و در حدود 7 میباشد. رسانایی ویژه آن (عکس مقاومت) بسیار کم میباشد. زیرا رسانایی الکتریکی آب با انحلال نمکها در آن افزایش مییابد. دمای جوش آن پایینتر از آبهای طبیعی میباشد و به علت عدم وجود مواد محلول خاصیت خورندگی ندارد.





 جواب بصورت نقل قول
جواب بصورت نقل قول


